5-Fu血藥濃度與藥代動力學參數AUC分布除去個別患者退組者(因患者治療後期依從性不高��
,部分患者未進行後續治療��
,對照組3例��
,實驗組3例)��
,37例對照組在6個周期內共計23次落在治療窗(AUC: 20~30mg·h /L) 的患者比例為16.67%(23/138) ��
,多數患者的5-Fu AUC值都低於治療窗範圍��
。實驗組基於 BSA 給藥後��
,患者的5-Fu血藥濃度分布也比較分散�
,第1周期落在治療窗範圍內的患者比例為21.6%(8/37) ��
,其變異係數(CV) 48.77%��
,經過2~6周期的劑量調整後�
,到第6周期時比例提升到67.74%(23/34)��
,其CV為22.75%��
。兩組間差異有統計學意義(χ2=20.04��
,P<0.01) ��
。對照組和實驗組6個周期內5-Fu血藥濃度分析結果見圖 1��
。
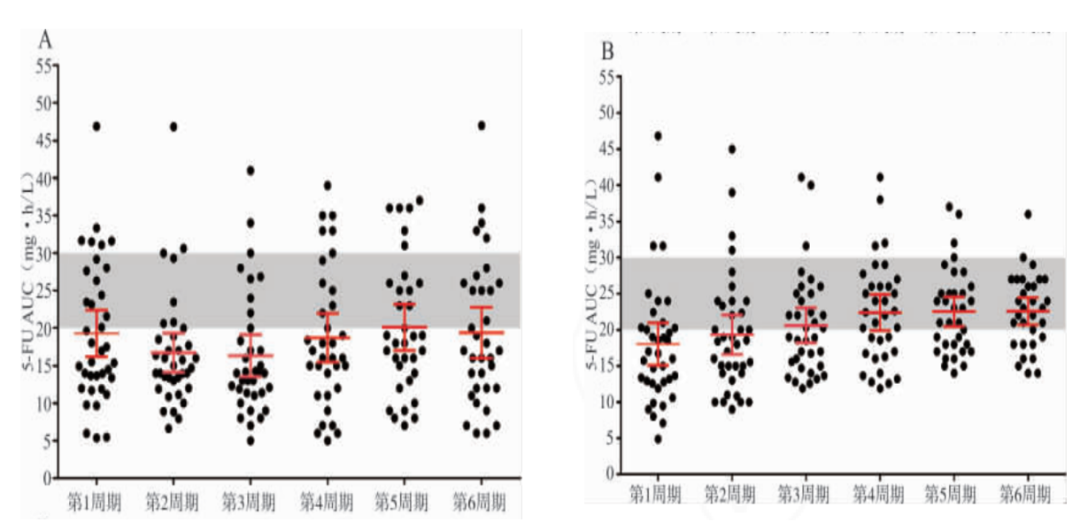
注:A��
,對照組多數患者的5-Fu AUC 值低於治療窗範圍��
。B��
,實驗組患者5-Fu血藥濃度落在治療窗範圍內的數量增加��
,且具有集中趨勢[5]�
。圖 1 對照組和實驗組患者6個周期 5-Fu AUC 分布情況
5-Fu毒副反應與劑量調整的關係與對照組[70.3%( 26 /37) ]相比��
,實驗組毒副反應(≥3級) 發生率[32.4% (12/37)]差異有統計學意義(χ2=10.60�
,P<0.01) �
。進一步分析具體的毒副反應結果表明��
,腹瀉��
、口腔黏膜炎等毒副反應的差異均有統計學意義(P均<0.05) ��
,而惡心��
、嘔吐��
、手足綜合征��
、食欲下降��
、體重下降��
、白細胞減少等差異均無統計學意義(P均>0.05)
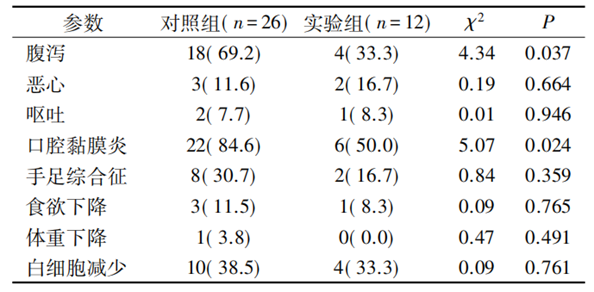
對照組與實驗組毒副反應的關係[n(%)]
大量針對西方人群的臨床試驗[6-7]表明��
,5-Fu的藥理特性與臨床毒性以及療效具有明顯的統計學相關性��
,而體表麵積給藥劑量與療效及總生存期差異均無統計學意義��
。這些臨床試驗表明��
,在結直腸癌治療領域中��
,通過對5-Fu常規血藥濃度監測�
,並根據每例患者的藥理表征進行個體化劑量調節��
,能夠實現降低毒性��
,增加治療效果的目的��
。5-Fu的有效治療濃度範圍(治療窗) 非常窄��
,患者對藥物的代謝差異��
,能引起個體藥效學上的巨大差異��
。因此��
,臨床迫切需要基於個體藥理差異對5-Fu進行血藥濃度監測及劑量調節[8]��
。
通過本研究結果對比可知��
,通過5-Fu血藥濃度檢測��
,及時調整患者的用藥劑量��
,可以使實驗組落在治療窗範圍內的患者比例明顯增加��
,表明通過藥代動力學進行5-Fu的劑量管理是一種臨床可行的操作��
。改變用藥劑量可能會帶來化療毒副反應增加的風險��
,但是本研究結果表明��
,通過劑量調整使得患者達到設定的治療窗血藥濃度範圍��
,不僅治療的效果沒有降低��
,反而在整體的毒性控製更優於BSA給藥方式��
。此外��
,本研究中以5-Fu為基礎的腸癌治療方案中��
,在引起白細胞減少症方麵差異無統計學意義(對照組為38.5%��
,實驗組為33.3%) ��,這與國外文獻的報道的結論類似[9]��
。
本研究亦證實通過監測患者化療過程中的5-Fu血藥濃度��
,可以預估患者本次化療的毒副反應發生情況�
,盡早予以幹預��。由於檢測的是5-Fu在靜脈持續滴注過程中的血藥濃度��
,因此��
,可以根據及時的檢測報告來預判本次5-Fu後續持續滴注過程中的代謝情況��
,進而可以依據患者自身狀態及檢測結果適當的進行滴注持續時間的調整�
,以控製化療相關毒性反應或者提高化療的療效��
。